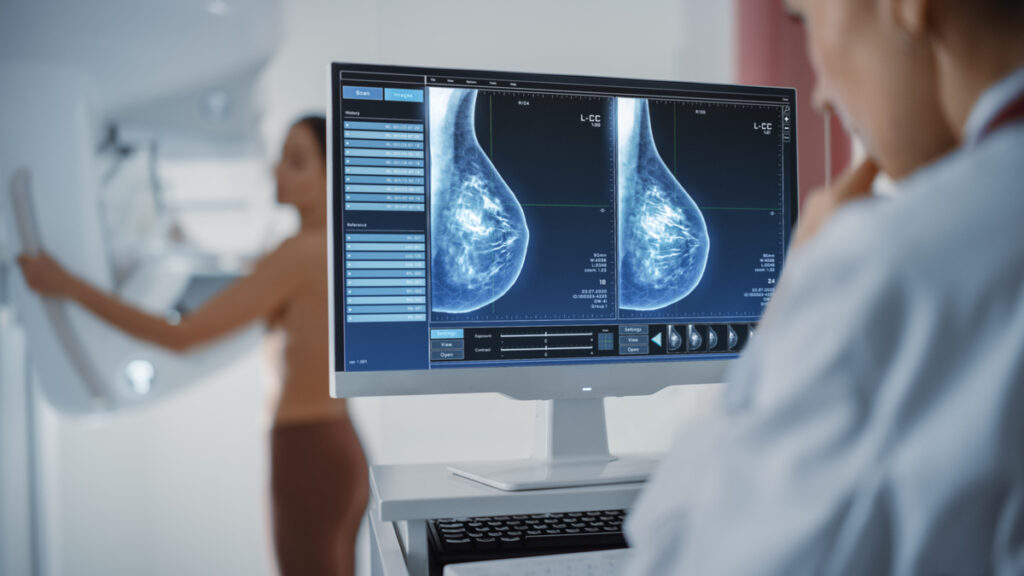
Computer Screen in Hospital Radiology Room: Beautiful Multiethnic Adult Woman Standing Topless Undergoing Mammography Screening Procedure. Screen Showing the Mammogram Scans of Dense Breast Tissues.
Enhertu (trastuzumab deruxtecán) se proyecta como la opción terapéutica más importante para pacientes oncológicos en los próximos años y ha demostrado mejora tanto en supervivencia sin progresión como en supervivencia general.
- 1 de cada 5 casos de cáncer de mama diagnosticados es HER2 positivoy en la mayoría de los casos se asocia con una enfermedad más agresiva.[3]
- Las Guías Internacionales colocan a Enhertu como “régimen preferido” para aquellas pacientes con cáncer de mama metastásico HER2 positivas. [4]
Febrero, 2024 (Ciudad de Panamá, Panamá) – Enhertu (trastuzumab deruxtecán / T-DXd) es el nombre del nuevo medicamento de AstraZeneca para personas diagnosticadas con cáncer de mama positivo para el receptor 2 del factor de crecimiento epidérmico humano (HER2) que no se puede extirpar mediante cirugía, que se ha diseminado a otras partes del cuerpo (metastásico), que han recibido un tratamiento anti-HER2 previo contra el cáncer de mama para enfermedad metastásica, o tiene un cáncer de mama que ha regresado durante o dentro de los 6 meses posteriores a completar el tratamiento para su cáncer de mama en etapa temprana[5].
Gracias a la evidencia generada en el estudio clínico DESTINY-Breast03 [6], las Guías Internacionales actualizaron recientemente la recomendación de tratamiento en segunda línea (tratamiento que se administra cuando el tratamiento inicial o de primera línea no es eficaz o deja de ser eficaz) y establecieron a Enhertu como “régimen preferido”[7], pues sus resultados reflejan números muy positivos, mostrando una supervivencia sin progresión de alrededor de 28 meses en comparación con el promedio de 7 meses que ofrecen otros tratamientos, lo que reduce un 67% la progresión de la enfermedad.[8],[9] Por su diseño, Enhertu además, es un medicamento menos tóxico para las células sanas y más eficaz contra las células cancerosas, manteniendo la calidad de vida durante el tratamiento.
Gracias a esta contundente data clínica, la Administración de Drogas y Alimentos de los Estados Unidos (FDA por sus siglas en inglés) dio trámite rápido de aprobación y puso a disposición de médicos y pacientes esta terapia innovadora para el abordaje del cáncer de mama metastásico HER2+, en pacientes con progresión de la enfermedad después de haber recibido un tratamiento previo con otras terapias anti-HER2.[10],[11]
Enhertu también demostró que ofrece una mejora, tanto en la supervivencia sin progresión (cantidad de tiempo que una persona vive sin que el cáncer avance), como en la supervivencia general (cantidad de tiempo que una persona vive con o sin crecimiento del cáncer) en personas diagnosticadas con cáncer de mama metastásico con niveles bajos de HER2 que han recibido una terapia sistémica previa en el entorno metastásico o desarrollado recurrencia de la enfermedad durante o dentro de los seis meses posteriores a la finalización de la quimioterapia adyuvante, basado en la evidencia clínica del estudio DESTINY-Breast04. Esto representa un nuevo paradigma de tratamiento y esperanza para estos pacientes.[12]
“Estamos orgullosos del gran avance que hemos logrado como una compañía de innovación, desafiando los límites de la ciencia y claros en el objetivo de erradicar el cáncer como causa de muerte. Enhertu cambiará la vida de muchos pacientes y sus familias, quienes tendrán la oportunidad de contar con más tiempo y tiempo de calidad, pues el tratamiento no solo ha demostrado ser muy eficaz, sino que es más tolerable para una persona que ha recibido múltiples terapias contra el cáncer,” explicó el Dr. Andrés Rojas, Director Médico de AstraZeneca para Centroamérica y Caribe.
El cáncer de mama sigue siendo el tipo de cáncer más frecuente a nivel mundial. Solo en el año 2020 se diagnosticaron aproximadamente 2 millones de casos[13], causando alrededor de 685 mil muertes en todo el mundo[14]. Del total de casos reportados, un 20% corresponde al tipo HER2 positivo[15] que en la mayoría de los casos se relaciona con una enfermedad agresiva e incurable, con una esperanza de vida más corta, con un pronóstico poco favorable para el paciente[16], y a diferencia de otros subtipos de cáncer de mama, tiene un mayor riesgo de desarrollar un segundo cáncer,[17],[18] generando una mayor carga clínica, emocional, social y económica para los pacientes, su núcleo familiar y para los sistemas de salud pública.[19],[20]
También es importante resaltar la importancia del nuevo paradigma de tratamiento en el caso de las pacientes con expresión baja de HER2, alrededor del 60% de los cánceres de mama metastásicos categorizados como negativos para HER2 expresan niveles bajos de HER2 (HER2-bajo) y esto hoy representa una oportunidad significativa ya que esta población previo al DESTINY-Breast04, se trataban como como si fueran pacientes con cáncer de mama metastásico HER2 negativo con opciones limitadas para las líneas posteriores de terapia.[21]
Poner esta información a disposición de la población es muy relevante. Se vuelve crítico identificar a los pacientes de alto riesgo con el objetivo de realizar un diagnóstico oportuno y una intervención temprana, mitigando así el impacto de la enfermedad.[22] “En AstraZeneca, ponemos a los pacientes primero, colocándolos en el corazón de lo que hacemos, para que puedan disfrutar de una mejor vida. A través de la investigación y el desarrollo de medicamentos de última generación, abordamos las necesidades médicas no cubiertas en distintos cánceres, lo que permite contar con opciones de tratamientos y mayor conocimiento, lo que nos permite transformar la vida de miles de pacientes alrededor del mundo y nuestra región no es la excepción,” concluyó el Dr. Rojas.
____________________________
AstraZeneca
AstraZeneca es una compañía biofarmacéutica global liderada por la ciencia que se enfoca en el descubrimiento, desarrollo y comercialización de medicamentos de prescripción, principalmente para el tratamiento de enfermedades en tres áreas terapéuticas: Oncología; Cardiovascular, Renal y Metabolismo y Respiratorio e Inmunología. Con sede en Cambridge, Reino Unido, AstraZeneca opera en más de 100 países y sus medicamentos innovadores son utilizados por millones de pacientes en todo el mundo. Visite https://www.camcar.astrazeneca.com/es/ y siga a la Compañía en Twitter @AstraZenecaCAM.
Contacto de prensa:
Mónica Solórzano Lobo- monica.solorzano1@astrazeneca.com
External Affairs and Communications Lead, AstraZeneca Central American and Caribbean
[1] Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. New England Journal of Medicine. 2012;367(19):1783-91.
[2] Daiichi-Sankyo Inc. A. DS8201-A-U302 Clinical Study Report (CSR). Interim Analysis 2. Data on file2022.
[3] Pillai R, et al. Cancer. 2017;1;123(21):4099-4105.
[4] Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. New England Journal of Medicine. 2012;367(19):1783-91.
[5] https://www.enhertu.com/en/breast. Última visita realizada en enero de 2024.
[6] Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. New England Journal of Medicine. 2012;367(19):1783-91.
[7] Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. New England Journal of Medicine. 2012;367(19):1783-91.
[8] Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. New England Journal of Medicine. 2012;367(19):1783-91.
[9] Daiichi-Sankyo Inc. A. DS8201-A-U302 Clinical Study Report (CSR). Interim Analysis 2. Data on file2022.
[10] Inc. D-S. FDA grants breakthrough therapy designation to Daiichi Sankyo’s DS-8201 for HER2-positive metastatic breast cancer. 2017.
[11] U.S D-SI. FDA grants fast track designation for HER2-targeting antibody drug conjugate DS-8201 for HER2-positive metastatic breast cancer. 2016.
[12] Modi Set al. N Engl J Med. 2022;387 (1): 9-20.
[13] World Health Organization. (2020). Cancer today. Global Cancer Observatory. Recuperado 16 de enero de 2024, de https://acortar.link/VVtovq
[14] World Health Organization. (2020). Cancer today. Global Cancer Observatory. Recuperado 16 de enero de 2024, de https://acortar.link/VVtovq
[15] Ahn S, et al. J Pathol Transl Med. 2020; 54(1): 34-44.
[16] Pillai R, et al. Cancer. 2017;1;123(21):4099-4105.
[17] Uzunoğlu S. Overcoming the resistance in HER2(+) metastatic breast cancer. Leukemia Research. 2019;85(2019):S15-S.
[18] Hu ZY, Xiao H, Xiao M, Tang Y, Sun J, Xie ZM, et al. Inducing or Preventing Subsequent Malignancies for Breast Cancer Survivors? Double-edged Sword of Estrogen Receptor and Progesterone Receptor. Clinical Breast Cancer. 2018;18(5):e1149–e63111
[19] Zimmer AS, D Van Swearingen AE, Anders CK, Carey Anders CK, Duke Health Scholar T. HER2-positive breast cancer brain metastasis: A new and exciting landscape. 2020
[20] C P, Ln H, Mr S. Use of biomarkers to guide decisions on systemic therapy for women with metastatic breast cancer: American society of clinical oncology clinical practice guideline. Journal of Oncology Practice. 2015.
[21] Tarantino P et al. J Clin Oncol. 2020; 38 (17):1951-1962. 2. Aogi K et al. Ann Oncol. 2012; 23: 1441- 1448. 3. Eiger D et al. Cánceres (Basilea). 2021; 13(5): 1015. 4. Fehrenbacher Let al. J Clin Oncol. 2019; 38 (5): 444-453
[22] Powell CA, et al. Póster presentado en la Reunión Anual Virtual de la AACR; 10 al 14 de abril de 2021. Póster CT167.
Producido por AstraZeneca CAMCAR Costa Rica S.A., Roble Corporate Center, 5to piso. Escazú, San José, Costa Rica. Teléfono (506) 2201-3400, Apdo.: 0993-1260 Escazú. www.astrazeneca.com para AstraZeneca CAMCAR S.A. Para reporte de eventos adversos, quejas de calidad o información médica, visite https://www.contactazmedical.astrazeneca.com CC-11514 ENE-025






